| Статистика |
 |
| Наш опрос |
Оцените мой сайт
Всего ответов: 54
|
|
|
Вирусные заболевания пчел .
| |
| ВИК | Дата: Вторник, 04.05.2021, 12:37 | Сообщение # 16 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| После занесения V. destructor в Европу ABPV стал обнаруживаться с высокой интенсивностью заражения в сильно заклещеванных семьях, где регистрировался погибший запечатанный и незапечатанный расплод. Впервые на эту проблему обратили внимание в России и Германии в конце 1970-х—начале 1980-х годов (74). Затем аналогичные сообщения были опубликованы учеными из Нидерландов, Италии, бывшей Югославии, Франции (71), Венгрии, Австрии (52), Дании (37) и США (72). В Германии и Голландии частота выявления ABPV у мертвых пчел в семьях со слабой, средней и высокой степенью заклещеванности составляла соответственно 3; 44 и 80 %. Интересно, что в Англии ABPV не обнаружили в семьях, свободных от клеща.
Во Франции ABPV были инфицированы 58 % взрослых пчел, 23 % куколок и внешне здоровых пчел, а у клеща Varroa этот показатель составил 36 %. Инфицирование пчел вирусом чаще наблюдалось в заклещеван-ных семьях в конце лета и осенью, что коррелировало с пиком роста популяции клеща Varroa (10). Исследования на пасеках в Дании (75) показали заражение 14 % пчелосемей, что отличается от данных по Франции и Австрии (58 % у клинически здоровых и 68 % — у больных пчел) (52).Датские ученые предполагают, что такие результаты могут объясняться тем, что в борьбе с клещом используются органические кислоты. Они менее эффективны против варрооза, и пчелам приходится бороться с большей заклещеванностью, что приводит к естественной убыли особей, зараженных вирусом. В 2004 году в Дании ABPV был выявлен с экстенсивностью 73 %, а в 2005 — 80 % (76). Эти исследования позволили найти взаимосвязь между инфицированностью, заклещеванностью и гибелью семей зимой. Статистически значимая зависимость между частотой выявления ABPV перед зимовкой и гибелью семей зимой была показана для сезонов 2005-2006, но не 2004-2005 годов. Однако степень заклещеванности и гибель семей зимой коррелировали в обоих случаях. Можно предположить, что клещ Varroa способен передавать и активировать латентный ABPV, что служит одним из факторов гибели пчелосемей в период зимовки (76).
Кашмирский вирус и вирус израильского паралича. KBV впервые был описан в 1977 году у A. cerana (77). Это РНК-содержащий вирус, который при инокуляции в гемолимфу A. mellifera накапливается в высоких титрах (78). Инфицированные пчелы погибают в течение 6 сут при непосредственном попадании KBV в гемолимфу, но остаются внешне здоровыми при его скармливании (78). Очевидно, что летальность KBV зависит от пути передачи (78, 79). При этом ключевую роль в трансмиссии играет клещ Varroa. Впервые KBV выделен из гомоге-ната рабочих особей A. mellifera, экспериментально зараженных экстрактом A. cerana из Кашмира (Индия) (78). Очень интересен факт выявления KBV в популяции медоносных пчел A. mellifera в Австралии, поскольку A. cerana, которая, по-видимому, выполняет роль главного хозяина KBV, на этом континенте отсутствует. Затем KBV был выявлен у A. mellifera из Канады и Новой Зеландии (80), на острове Фиджи (81), США (49), Европе и Океании (35, 36, 82). В настоящее время KBV регистрируется у A. cerana (35, 77, 78), A. mellifera, шмелей (B. terrestris, B. pascuorum) и ос (Vespula germanica). В Северной Америке и Новой Зеландии в популяции медоносной пчелы инфицирование кашмирским вирусом превалирует над зараженностью другими вирусами (72, 83, 84), но в Европе этот вирус обнаруживается редко (10, 52, 82, 85).
Вирус поражает пчел на всех стадиях жизненного цикла и обычно сохраняется в расплоде латентно.
Еще один опасный вирус, близкородственный KBV, — вирус израильского паралича, который был обнаружен в Израиле после инокуляции здоровой личинке пчелы гомогената от мертвой пчелы (86). Поскольку симптомы оказались схожими с описанными при заражении вирусом острого паралича, этот патоген был назван вирусом израильского паралича пчел (Israeli acute bee paralysis virus, IAPV). Вирус широко распространен на Ближнем Востоке (86), в Австралии, США (87-89) и редко обнаруживается в Европе (90).
KBV и IAPV близкородственны и принадлежат к семейству Dic-istroviridae. Вместе с ABPV они формируют общий генетический комплекс со сходными путями передачи. Латентно присутствуя у пчелы на стадии личинки, они вызывают быструю гибель взрослой особи с характерными клиническими признаками. Генетический анализ KBV и ABPV показал наличие около 70 % генетической гомологии, однако между ними имеются и различия (91).
ABPV, KBV и IAPV в низких титрах могут постоянно присутствовать у пчел без развития клинических признаков (72, 89). Когда количество KBV и IAPV достигает предельных значений, происходит гибель зараженных пчел (77, 86, 88). Повышение титра вирусов в гемолимфе пчелы при естественном заражении связано с клещом Varroa, который служит вектором и одновременно активатором их репликации(49, 92, 93).
|
| |
| |
| ВИК | Дата: Вторник, 04.05.2021, 12:37 | Сообщение # 17 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| Изучение путей передачи KBV и IAPV (42, 51, 94) показало важную роль V. destructor в проявлении патогенности KBV, однако точные механизмы патологии остаются неизученными (42). Существует мнение, что V. destructor подавляет иммунную защиту пчел, приводя к активации постоянно присутствующих в организме пчелы вирусов (19). Другие исследователи считают, что V. destructor служит вектором, который напрямую переносит KBV куколкам, поскольку KBV был найден в слюне клеща (42). Более того, заражение клеща и передача KBV расплоду доказана экспериментально (95). Установлена эффективность передачи KBV расплоду через V. destructor, которая составила 70 %(эффективность переноса вируса от клеща к клещу или заражения клеща от расплода 51 %). KBV играет ключевую роль в гибели заклещеванных семей (72, 77). Вирулентность IAPV также, по-видимому, связана с V. destructor. Присутствие IAPV является маркером так называемого коллапса пчелиных семей в США, который характеризуется следующими признаками: мертвые пчелы на дне улья или рядом с ним отсутствуют, пчелы оставляют расплод и матку, при достаточном количестве кормов масса рабочих пчел в улье критически снижается (96). Важно отметить, что IAPV распространен и в Австралии, но при этом коллапса пчелиных семей там не наблюдалось. Изучение коллапса семей в США (97) и гибели семей во время зимовки без признаков коллапса в Германии (76) выявило сложную зависимость между представителями комплекса ABPV-KBV-IAPV и V. destructor, причем активатором латентных инфекций выступает именно клещ. Перечисленные три вируса имеют разное географическое распространение (98), и этим объясняется, почему IAPV или KBV могут вызывать гибель семей в США, а ABPV — в Европе.
Известно (пока только для одного из этих вирусов), что IAPV может интегрироваться в геном пчелы. Так, геном около 30 % живых пчел в Израиле имеет в своем составе встроенную частичную последовательность генома IAPV (86). Последовательность генома IAPV также выявлена в составе генома клеща Varroa. Более того, пчелы с интегрированным геномом IAPV приобретают устойчивость к заражению этим вирусом (86).
Вирус черного маточника. BQCV впервые выделили из почерневших личинок и предкуколок пчел, ячейки которых также были черными (78). BQCV поражает в основном личинок и куколок маток медоносных пчел в запечатанных ячейках. Пораженные личинки имеют бледно-желтый цвет и покрыты плотной кожицей в виде мешочка, что характерно для мешотчатого расплода. Размножение BQCV в куколках маток вызывает их почернение и быструю гибель. Затем чернеет и сам маточник. Рабочие пчелы также могут заразиться, однако у них инфекция внешне не проявляется. Более того, BQCV не реплицируется в пчелах при алиментарном заражении.
Вирус черного маточника зарегистрирован в Северной Америке, Европе, Океании, Азии, Африке, Ближнем Востоке и Азербайджане (31, 35, 36). По результатам 5-летних исследований в городе Белтсвиль (MD, США) установлено, что BQCV — второй из наиболее распространенных вирусов медоносных пчел после вируса деформации крыла DWV (27). В Австралии BQCV — наиболее частая причина гибели маток во время развития.
В результате исследований взрослых пчел и куколок (10) установлено, что BQCV распространен у взрослых особей и чаще наблюдается в весенний и летний периоды.
Существует взаимосвязь между зараженностью пчел вирусом черного маточника и инфицированностью микроспоридией Nosema apis: при широком распространении N. apis возрастает частота выявления BQCV на той же территории. Репликация вируса в пчелах, зараженных N. apis, происходит намного быстрее, чем в незараженных.
Предполагается, что BQCV передается матке во время скармливания ей маточного молочка пчелой-кормилицей. N. apis поражает кишечник, создавая условия для инфицирования BQCV. Во всех частях Англии и Уэльса рабочие пчелы, зараженные BQCV, были одновременно коинфи-цированы N. apis (8). На пасеках в Австрии N. apis обнаружили в 78 % образцов, положительных по BQCV; у 75 % инфицированных N. apis пчелиных семей был выявлен BQCV. Аналогичные результаты получили во Франции (10).
Было высказано предположение, что клещ варроа может служить вектором для BQCV. Обнаружение BQCV в теле клеща на пасеках в Таиланде подтверждает эту гипотезу (56), в то же время в других исследованиях (10) этот вирус в клеще варроа не был выявлен.
|
| |
| |
| ВИК | Дата: Вторник, 04.05.2021, 12:39 | Сообщение # 18 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| Вирус хронического паралича пчел. Ранее трахейный клещ Acarapis woodi считался причиной паралича у пчел, однако в конце 1960-х годов было установлено, что у взрослых пчел паралич имеет вирусную этиологию, и впоследствии каузальный агент получил название вируса хронического паралича — CBPV. В настоящее время CBPV выявлен у рабочих пчел практически повсеместно, за исключением Южной Америки (35, 36). Вирус хронического паралича при низкой интенсивности часто обнаруживается у внешне здоровых пчел вместе с ABPV. По сравнению с ABPV вирус хронического паралича менее вирулентен: при инфицировании CBPV требуется несколько суток, чтобы вызвать гибель пчелы, а в случае ABPV это происходит за одни сутки.
Заражение вирусом хронического паралича пчел сопровождается, как правило, симптомами двух типов. Наиболее выраженные — дрожание тельца и крыльев, ползание по земле из-за неспособности летать, раздутое брюшко и расставленные крылья. Еще одна форма — отсутствие ворсинок и почернение тельца. Таких особей пчелы изгоняют из улья. Обе формы симптомов могут наблюдаться в одной и той же пчелосемье.
Для оценки инфекционных свойств вируса хронического паралича в гемолимфу пчел вводили вирусный препарат, наносили его на поверхность тела пчелы или добавляли в корм. Было установлено, что CBPV легко проникает через кутикулу насекомых при отсутствии ворсинок, однако в случае перорального заражения репликация вируса в организме пчелы минимальна и не приводит к смерти. Облегчает проникновение вируса через кутикулу теснота в улье при несвоевременном расширении гнезд. Заражение этим вирусом происходит при наличии двух факторов. Первый — плохие погодные условия, при которых пчелы не вылетают из улья. Этим объясняют более высокую распространенность вируса хронического паралича во Франции (99). Второй фактор связан с используемыми технологиями пчеловодства. Так, увеличение площади посева подсолнечника во Франции и, как результат, обильный монофлерный взяток, привел к быстрому уменьшению внутриульевого пространства, которое не было своевременно расширено, в результате чего произошла гибель семей с типичными признаками хронического паралича (100). Распространение CBPV в мире неравномерно. В Британии он встречается очень часто и вызывает гибель пчелосемей (8), в Австрии его обнаружили только у 10 % пчелосемей (52), во Франции CBPV распространен не более чем у 4 % семей. Важно отметить, что для CBPV не характерна сезонная динамика (10). Наиболее вероятно распространение CBPV посредством проникновения через кутикулу. В Таиланде и во Франции проводилось обследование пчел и клещей Varroa на наличие вируса CBPV, при этом пчелы были инфицированы, но клещи оказались свободными от вируса (27). Еще в одном исследовании, выполненном во Франции, CBPV обнаружили у муравьев (Camponotus vagus и Formica rufa) и клеща V destructor, причем реплика-тивно активную РНК-цепь выявили у C. vagus и V destructor, что доказывает роль последнего как биологического вектора CBPV. Обнаружение CBPV у C. vagus предполагает возможность его распространения через муравьев, однако прямых доказательств этому нет. Муравьи могут заражаться, поедая инфицированных вирусом пчел, а также пчелы и муравьи могут заражаться, поедая падь зеленой пихтовой тли Cinara pectinatae. Однако у тли CBPV к настоящему времени не обнаружили. Следовательно, существуют не изученные пока резервуары CBPV, которые служат источником инфицирования муравьев (101).
|
| |
| |
| ВИК | Дата: Вторник, 04.05.2021, 12:40 | Сообщение # 19 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| Вирус мешотчатого расплода. SBV широко распространен в популяциях медоносной пчелы на всех континентах (35, 36). Вирус поражает пчел на всех стадиях жизненного цикла, но наиболее чувствителен к нему 2-суточный расплод. Вирусная инфекция у взрослых пчел развивается без клинических проявлений, но сокращает продолжительность жизни особей. SBV распространяется, когда ульевые пчелы начинают выбрасывать зараженных личинок. Вирус накапливается в слюнных железах пчелы, а затем разносится внутри колонии при кормлении расплода и обмене кормом. Молодые личинки заражаются, потребляя инфицированный корм. Вирус начинает реплицироваться на личиночной стадии пчелы, вызывая пожелтение личинок после запечатывания расплода. При прогрес-сировании заболевания кутикула становится жесткой и личинка не в состоянии окуклиться. Вирус накапливается в большом количестве под личиночной кутикулой (1, 102).
Зараженность SBV, как правило, носит сезонный характер с доми-
нированием весной и летом (8, 10). При мешотчатом расплоде, как и при гнильцовых инвазиях, рабочие пчелы обычно удаляют погибших личинок либо съедают их, что приводит к дальнейшему распространению инфекции внутри улья. По отношению к больным личинкам в некоторых пчелосемьях гигиеническое поведение может быть ослаблено: здоровые насекомые узнают латентно зараженных мешотчатым расплодом личинок до того, как произойдет нарастание количества вируса в мумифицированных пчелах и проявятся симпотомы (103).
О роли клеща Varroa в трансмиссии SBV сообщается в многочисленных публикациях о выявлении вируса у летных пчел с высокой закле-щеванностью (52, 73), а также в организме самих клещей (10, 42, 56).
Профилактика вирусных заболеваний у пчел. Согласно экспериментальным данным, вирусы ABPV, BQCV, CBPV, DWV, KBV и SBV могут обнаруживаться в пыльце, BQCV и DWV — дополнительно еще в меде, ABPV, CBPV, KBV и SBV — в перге (однако отсутствуют в слюне пчел и маточном молочке) (63). По данным других авторов, KBV и SBV обнаруживали в маточном молочке, а также в меде и пыльце (42).
Обнаружение вирусов у V. destructor указывает на его ключевую роль в трансмиссии каузального агента в заклещеванной пчелосемье (10, 21, 32, 51, 56, 66). Установлено, что тяжелые инфекции, вызванные вирусами ABPV, CBPV, медленного паралича (slow paralytic virus, SPV), BQCV, KBV, затемненного крыла (cloudy wing virus, CWV), SBV и DWV, которые приводят к развитию клинических признаков и гибели особей, были зарегистрированы в пчелосемьях с высокой заклещеванностью (10, 104). Дополнительные исследования показали, что эффективность трансмиссии вируса зависит от численности клеща в ячейке и, как следствие, от заклещеванности колонии. Более того, наличие в ячейке инфицированных и неинфицированных клещей приводит к тому, что неинфициро-ванные клещи также заражаются через гемолимфу зараженной куколки. Этот факт не оставляет сомнения, что высокая заклещеванность представляет угрозу для пчеловодства во всем мире.
|
| |
| |
| ВИК | Дата: Вторник, 04.05.2021, 12:41 | Сообщение # 20 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| В настоящее время существует три направления исследований по обозначенной проблеме: разработка методов борьбы с клещом, селекция пород пчел А. mellifera, устойчивых к клещу, и обработка пчел против вирусных инфекций. Перечисленные подходы необходимо применять в комплексе, поскольку при проведении метагеномных исследований пчелиных семей, которые подверглись коллапсу, и тех семей, которые выжили, установлено, что основными маркерами коллапса пчелиных семей служит присутствие V. destructor вместе с IAPV и DWV (91).
Для снижения вероятности гибели пчелосемей необходимо контролировать популяцию клеща Varroa (105). Поскольку клещ активирует скрытые вирусные инфекции, ослабляет иммунитет и нарушает обмен веществ, то сдерживание заклещеванности служит залогом благополучия пчелосемей. В отсутствие клеща и при благоприятных условиях внешней среды вирусные инфекции не представляют опасности для пчел (106). Вирусы пчел могут быть идентифицированы в теле трутня (95), в сперме трутней (63, 107), а также в сперматеке маток (68), что предполагает вертикальный путь передачи вирусов потомству и вероятность заражения матки во время спаривания. Поскольку матки в течение жизни откладывают десятки тысяч яиц, вертикальная передача инфекции может представлять серьезный риск для пчелиной колонии, угрожая ее выживанию, что указывает на важность регулярной и своевременной замены маток.
Попытки селекции устойчивых к клещу Varroa пород пчел делаются, но пока удовлетворительных результатов не принесли. Наблюдения за 150 пчелосемьями в течение 6 лет без применения акарицидов и с возможностью свободного роения показали, что на 3-й год гибель пчелосемей зимой достигла 80 %, но снизилась до 12-18 % в течение последующих 2 лет. В итоге в последний год осталось только 11 семей (108). Во Франции в течение 7 лет проводили наблюдения за 82 пчелосемьями (без обработки акарицидами), сравнивая их с семьями, которые обрабатывали акарицида-ми. По вариантам смертность семей во время зимовки статистически значимо не различалась, однако сбор нектара в необработанных семьях был на 41 % ниже. Таким образом, более устойчивые к клещу пчелы имели меньшую медопродуктивность, что не выгодно экономически (109).
Лечение вирусных инфекций пчел в настоящее время возможно с помощью малых интерферирующих РНК (микроРНК, миРНК) по принципу посттранскрипционного сайленсинга, связываясь с матричной РНК вирусов, приводя к деградации последних (110, 111). Источником миРНК является сама вирусная РНК, которая реплицируется через образование дцРНК (112, 113). В то же время в недавнем исследовании по применению принципа нокаута генов для борьбы с IBPV продемонстрирована эффективность этого подхода — процент гибели пчелосемей снижался (114). Оказалось, что при скармливании пчелам дцРНК вируса последняя активирует деградацию вирусной РНК IBPV. Однако проблема создания таких препаратов заключается в высокой себестоимости производства и сложности их целенаправленной доставки в органы и ткани насекомого. Аналогичный подход был применен для купирования симптомов при инфици-рованности DWV. Так, скармливание зараженным пчелам дцРНК DWV блокировало у них репликацию DWV (115). В качестве еще одного потенциально эффективного способа борьбы с вирусными инфекциями пчел рассматривается применение РНКаз. Например, РНКазы могут инактиви-ровать ABPV при предварительной инкубации in vitro суспензии вируса с препаратами РНКаз. Последующее заражение личинок обработанной вирусной суспензией не оказывало негативного влияния на зараженных личинок (115). Однако сохраняется более сложная задача — найти способ доставки этих препаратов в гемолимфу пчел.
|
| |
| |
| ВИК | Дата: Вторник, 04.05.2021, 12:42 | Сообщение # 21 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| Итак, из обнаруженных вирусов у медоносной пчелы наибольшее значение имеют вирус деформации крыла (DWV), вирус острого паралича (ABPV), вирус хронического паралича (CBPV), кашмирский вирус (KBV), вирус мешотчатого расплода (SBV), вирус черных маточников (BQCV). Вирусы ABPV, BQCV, CBPV, DWV обнаруживают в пыльце, BQCV и DWV — еще и в меде, ABPV, CBPV, KBV и SBV — в перге, меде, пыльце и маточном молочке. Показанная в многочисленных публикациях корреляция между накоплением большого количества перечисленных вирусов в организме пчел и их высокой заклещеванностью Varroa destructor указывает на то, что клещ выполняет роль агента, предрасполагающего к инфицированию пчел вирусами или активации у них латентной вирусной инфекции. Вирусы, попадая в организм пчел per or, в большинстве случаев не приводят к летальному исходу, тогда как при векторной передаче с участием V. destructor они вызывают массовую гибель пчел в течение короткого времени.Кроме того, для предотвращения проявления так называемого синдрома медоносных пчел, вызванного клещом-паразитом Varroa (bee parasitic mite syndrome), необходимо учитывать местные климатические особенности и то, какие методы пчеловодства применяются.
А.В. СПРЫГИН, Ю.Ю. БАБИН, Е.М. ХАНБЕКОВА, Л.Е. РУБЦОВА
https://u.to/7HlLGw
|
| |
| |
| ВИК | Дата: Воскресенье, 21.11.2021, 23:36 | Сообщение # 22 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| При укусе пчелы клещом-носителем вируса, а клещи почти все носители, вирус попадает в организм пчелы через рану, где нет ему никакого противодействия. Он быстро размножается в организме укушенной пчелы(куколки) до болезненных титров. Дальше эта пчела начинает "раздавать" высокие титры вирусов своим соплеменницам и расплоду. И это уже огромные титры. с которыми уже не справляется иммунитет . Тогда уже вирус может распространяться по семье и без участия клеща, и тоже вызывать открытую форму заболевания.
Если клеща в семье мало, то и укушенных им пчёл мало, а значит и открыто заболевших пчёл мало. Мало активно заболевших - низкая скорость распространения. Опять же здоровые пчёлы семьи перестают с больными пчёлами контактировать , что создаёт дополнительную изоляцию. Сами больные пчёлы тоже стараются быстрее покинуть улей.
|
| |
| |
| Selt | Дата: Вторник, 08.11.2022, 13:00 | Сообщение # 23 |
|
Лейтенант
Группа: Пользователи
Сообщений: 76
Статус: Offline
| Развитие(клинические проявления) КПС зависят от титров(количества) вирусов в личинках и телах пчёл, на разных стадиях поражения расплода, и взрослых пчёл. Т.е., в больном КПС улье могут быть пчёлы как с внешними, заметными признаками поражения тела, так и внешне нормальными. Пчеловоды обычно ориентируются на деформированные крылья пчёл при КПС, но сейчас очень часто встречается "ползучка" пчёл с нормальными крыльями. Пчёлы просто не могут взлететь из-за повреждения вирусом ВДК других органов. А многие пораженные вирусом пчёлы вполне могут летать, и даже не один день, но продолжительность их жизни сокращена в разы. Т.е., вирус тоже меняется, и приобретает новые характеристики, меняется и проявление КПС. Потому КПС и остаётся пока СИНДРОМОМ, а не БОЛЕЗНЬЮ, не нозологической единицей, как, например, АГ.
При низких титрах будет ещё не болезнь, а вирусоносительство.
Дальше...Титры вирусов и скорость их нарастания в организме носителя зависят как от внешних факторов, так и от сопротивляемости(иммунитетом) пчёл.
|
| |
| |
| Selt | Дата: Пятница, 11.11.2022, 21:32 | Сообщение # 24 |
|
Лейтенант
Группа: Пользователи
Сообщений: 76
Статус: Offline
| Некоторые вирусы являются исторически и эволюционно постоянно присутствующими для пчел, то есть в той или иной комбинации независимо от клеща и пчеловода. Таких постоянно присутствующих вирусов 4-6
Повышенное внимание к вирусу деформации крыльев (DWV) связано с двумя факторами: 1) наглядность проявления заболевания; 2) наличие высокого титра в резко ослабевающих семьях, что позволило связать этот вирус с коллапсом пчелиных семей
Наличие вируса DWV обязательно для успешного развития клеща варроа. Повидимому этот вирус подавляет иммунную реакцию пчел на белки слюны клеща.
Присутствие вируса DWV в репликах медоносной пчелы Apis mellifera и ее подвидов регистрируется в 70-99% случаев, а у восковой пчелы Apis cerana, где клещ варроа не оказывает столь негативное влияние на семью пчел, регистрируется только в 0,1-0,7% случаев, то есть более чем в 100 раз реже.
5. Среди вирусов пчел существует неустойчивое равновесие. Так вариант А вируса DWV способен контролировать и даже подавлять более вирулентный вариант В. Вирусы ABPV и CBPV (вирус острого паралича пчел и вирус хронического паралича пчел) в свою очередь подавляют развитие вируса DWV
|
| |
| |
| ВИК | Дата: Четверг, 11.05.2023, 20:47 | Сообщение # 25 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| Вопрос применения трутовиков против вирусов пчел гораздо сложнее и часть очень важных моментов остаются за скобками. Возьмем три вида
трутовиков, о которых больше всего разговоров. Это Траметес разноцветный
(Trametes versicolor), Трутовик березовый (Piptoporus betulinus) и Трутовик
обыкновенный, или «копыто" (Fomes fomentarius).Содержание бэта глюканов 99, 95 и 90% соответственно.Казалось бы прекрасно, но антивирусная активность бэта глюканов зависит от типа
гликозидных связей 1-3, 1-4 или 1-6. Так вот, первые два типа приводят к
разветвленной конфигурации глюканов и увеличению молекулярной массы, что
неприемлемо для целей борьбы с вирусами, лучший вариант это 1-6 бэта глюканы.
Почему? Ответ достаточно прост и кроется в механизме взаимодействия с капсидом
вируса. Напомню, что воскообразную оболочку туберкулезной палочки, хотя это
бактерия а не вирус, состоящую их сложных полисахаридов способны разрушить
специальные ферменты (например трегалаза) отсутствующие у человека, но
имеющиеся у насекомых. В случае с вирусами механизм обратный. Простые бэта
глюканы способны инактивировать специальные белки капсида вирусов, препятствуя
репликации. Так сколько же этих простых водорастворимых глюканов среди 90-99%
всех бэта глюканов? Точного ответа до сих пор нет.
Трутовик обыкновенный и еще один трутовик под названием Ganoderma resinaceum помогают домашним пчелам бороться с вирусом деформированного крыла и вирусом Лейк Синай (LSV – Lake Sinai virus). До сих пор с вирусами боролись, стараясь избавить ульи от паразитических клещей варроа, которые их переносят. Однако грибы, возможно, окажутся более эффективным средством: если пчел поили сладкой водой с экстрактом из трутовиков, они намного реже заражались как вирусом деформированного крыла, так и LSV. Чем больше насекомые получали экстракта, тем устойчивей они были к вирусам: в случае с вирусом деформированного крыла заражение удавалось уменьшить в несколько раз .
В этом направлении я сейчас веду экспериментальную работу . Буду смотреть результаты .
|
| |
| |
| ВИК | Дата: Среда, 07.06.2023, 22:12 | Сообщение # 26 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| Экстракты мицелия полипоровых грибов уменьшают количество вирусов у медоносных пчел
Двумя наиболее важными факторами, способствующими массовой гибели колоний, являются заражение A. mellifera паразитическим клещом-разрушителем Varroa и набором ассоциированных вирусов5,6,7. Степень, в которой клещи варроа участвуют в усилении и распространении РНК-вирусов среди популяций медоносных пчел, стала очевидной только недавно, поскольку в настоящее время известно, что заражение варроа связано по меньшей мере с 10 вирусами медоносных пчел8,9,10. Признано, что вирусы играют важную роль в широко распространенных потерях колоний, особенно вирус деформированного крыла (DWV) и вирус-деструктор Варроа-1 (VDV1)6,7,11,12,13. DWV - это разрушительный вирус, который вызывает сморщивание крыльев, сокращение продолжительности жизни рабочих, уменьшение количества корма и подавление иммунитета у медоносных пчел14,15 (рис. 1A). В дополнение к передаче, опосредованной клещами, РНК-вирусы (включая DWV) также могут передаваться среди опылителей через пыльцу16,17. Другим потенциально проблемным вирусом, связанным с медоносными пчелами и клещами варроа, являются вирусы группы 9,18 вируса озера Синай. LSV был впервые выявлен в 201019 году, но в настоящее время широко распространен в колониях медоносных пчел
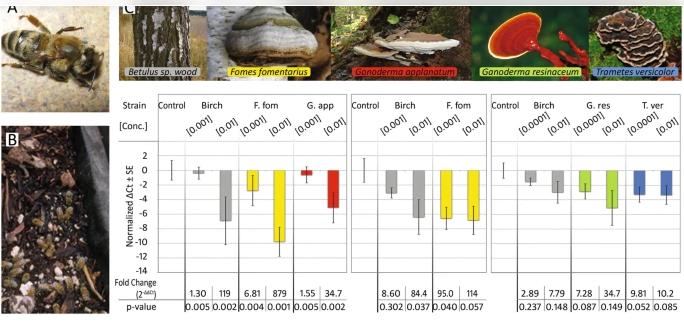
Экстракты из грибов снижают уровень вируса деформированного крыла (DWV) у медоносных пчел. (A) DWV сокращает продолжительность жизни рабочих и вызывает аномалии развития у медоносных пчел, включая деформацию крыльев. (B) Медоносные пчелы питаются мицелием грибов, где они поглощают жидкие экссудаты. © У пчел, которых кормили экстрактами из полипорового мицелия, наблюдались более низкие титры вируса DWV. В трех различных испытаниях смешивание экстрактов грибов с сахарозным сиропом для пчел в клетках значительно снижало уровни DWV, определенные методом qPCR. Примечательно, что экстракты мицелия F. fomentarius снижали уровень DWV более чем в 800 раз в первом испытании (двуххвостый t-тест, n = 10, t = 1,12, p = 0,005). Для каждого испытания значения qPCR ΔCt нормализованы к среднему значению соответствующих контрольных групп. Фотографии: Xolani90-https://commons.wikimedia.org/wiki/File:Deformed_Wing_Virus_in_worker_bee.JPG - [CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0 )]-без изменений (A), PES (B, Fomes, G. resinaceum), Titus Tscharntke – Викисклад (Betula), Джордж Чернилевский-Викисклад (G. applanatum), Норберт Нагель -https://commons.wikimedia.org/wiki/File:Trametes_versicolor_-_Coriolus_versicolor_-_Polyporus_versicolor_-_Schmetterlingstramete_-_Bunte_Tramete_-_Schmetterlingsporling_-_01.jpg [CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0 )]-обрезанные (Trametes).
|
| |
| |
| ВИК | Дата: Четверг, 08.06.2023, 22:35 | Сообщение # 27 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
| Лабораторные эксперименты с пчелами в клетках показали, что пероральная обработка экстрактами мицелия древесных шишек значительно снижала уровень DWV. Эффект от обработки экстрактами грибов, независимо от вида, был весьма значительным по сравнению с пчелами в клетках, которых кормили только сахарным сиропом (контрольный уровень сахара DWV по сравнению с все обработки мицелием: двуххвостый t-тест, n = 58; t = 4,33, p = 0,0001, изменение ΔΔCt в два раза = 23,0). Экстракты Fomes fomentarius (рак амаду) и Ganoderma applanatum (рак художника) проявляли значительную противовирусную активность дозозависимым образом (рис. 1C). Самый эффективный экстракт, содержащий 1% (в /в) F. fomentarius экстракт: смесь сахарного сиропа, снизил DWV более чем в 800 раз у содержащихся в клетках медоносных пчел по сравнению с контролем сахарного сиропа (двуххвостый t-тест, n = 10, t = 1,12, p = 0,005, изменение ΔΔCt в 879 раз).Подобно DWV, LSV также широко распространен у медоносных пчел в Северной и Южной Америке и Европе9. Мы протестировали 36 отдельных пчелиных брюшек, полученных из исходной популяции, и обнаружили, что у 100% особей положительный результат теста как на DWV, так и на LSV (рис. 2A). LSV демонстрировал более высокие уровни вирусной нагрузки, чем DWV, и LSV часто экспрессировался более высоко, чем эталонный ген, используемый для qPCR (рибосомный белок 5). Обработка пчел в клетках экстрактами грибов снижала уровни LSV (рис. 2B), при этом F. fomentarius (двуххвостый t-тест, n = 8, t = 3,96, p = 0,009, изменение ΔΔCt в разы = 5,40) и T. versicolor (двуххвостый t-тест, n = 8, t = 3,28, p = 0,0136, изменение ΔΔCt в разы = 75) демонстрируют значительное снижение. Ganoderma resinaceum продемонстрировала наибольшее среднее снижение по сравнению с контрольными клетками (двуххвостый t-тест, n = 8, t = 2,59, p = 0,084, изменение ΔΔCt в разы = 499), но также и наибольшее различие среди протестированных экстрактов. Общий эффект обработки экстрактами грибов, независимо от вида, был весьма значительным по сравнению с пчелами в клетках, которых кормили только сахарным сиропом (контроль сахара LSV по сравнению с все обработки мицелием: двуххвостый t-тест, n = 33, t = 3,98, p = 0,0004, изменение ΔΔCt в разы = 21,1).
|
| |
| |
| ВИК | Дата: Суббота, 10.06.2023, 20:47 | Сообщение # 28 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
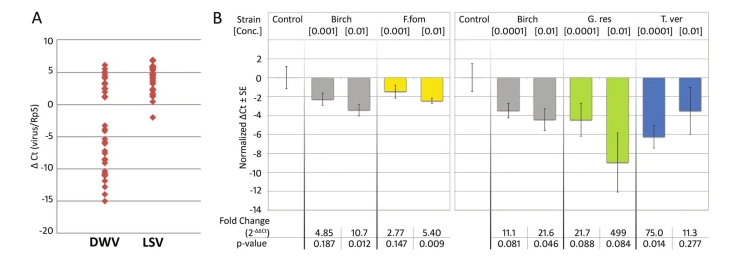
| Вирус озера Синай (LSV) уменьшается при обработке экстрактами грибов. (A) Все 36 особей пчелиных брюшек из нашей исходной популяции дали положительный результат как на DWV, так и на LSV. LSV был более высоко экспрессирован, чем DWV, и более высоко экспрессировался, чем эталонный ген медоносной пчелы RpS5. (B) Экстракты грибов снижали титры LSV у пчел после 7 дней обработки. F. fomentarius значительно снижал LSV при дозировке 1% (двуххвостый t-тест, n = 8, t = 3,96, p = 0,009, изменение ΔΔCt в разы = 5,40). Наибольшая разница в изменении в разы наблюдалась с экстрактом G. resinaceum, где обработка снижала уровень LSV у пчел в 499 раз по сравнению с пчелами, которых кормили только сиропом сахарозы (двухвалентный t-тест, n = 8, t = 2,59, p = 0,084).
Изображение в натуральную величину
Два экстракта, демонстрирующие наибольшее кратное снижение уровня DWV и LSV в клеточных исследованиях, были отобраны для валидации в полевых испытаниях. Небольшие экспериментальные колонии однократно обрабатывали 3 л 1%-ного экстракта грибов в растворе сахарозы 1:1 или только раствором сахарозы (рис. 3А). Количественный ПЦР-анализ показал, что как DWV, так и LSV были снижены в обработанных колониях через 12 дней (рис. 3B). Что касается DWV, то в ульях, обработанных экстрактом F. fomentarius, наблюдалось значительное снижение уровней вируса в 79,7 раза (двуххвостый t-тест, n = 18, t = 6,58, p = 6,32 × 10 -6, изменение ΔΔCt в разы = 79,7), что в 44 раза больше, чем в контрольных колониях. Экстракты G. resinaceum также значительно снижали уровни DWV (двуххвостый t-тест, n = 20, t = 9,75, p = 1,31 × 10-8, изменение ΔΔCt в два раза = 144), при этом обработанные колонии демонстрировали в 79,6 раза большее снижение вирусности, чем контрольные колонии. Лечебный эффект от экстрактов грибов был более выражен при LSV. Хотя в контрольных колониях наблюдалось некоторое снижение (двуххвостый t-тест, n = 18, t = 1,15, p = 0,267, изменение ΔΔCt в разы = 82,3), обработка F. fomentarius снизила уровень LSV на 87.в 9 раз больше, чем в контрольных колониях (двуххвостый t-тест, n = 18, t = 2,50, p = 0,0238, изменение ΔΔCt в разы = 7,380). Наибольшее снижение уровней вируса в этих экспериментах было при обработке G. resinaceum, где уровни LSV снижались в 45 000 раз больше, чем в контрольных колониях (двуххвостый t-тест, n = 20, t = 6,37, p = 5,34 × 10-6, изменение ΔΔCt в разы = 3,76 × 106).
|
| |
| |
| ВИК | Дата: Воскресенье, 11.06.2023, 22:43 | Сообщение # 29 |
 Admin
Группа: Администраторы
Сообщений: 1776
Статус: Offline
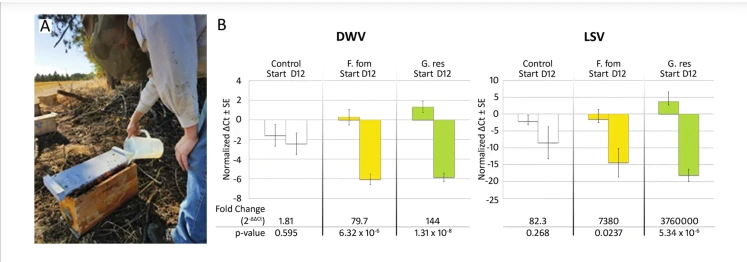
| Экстракты грибов снижают уровни DWV и LSV в полевых испытаниях. (A) Экстракты грибов смешивали с раствором сахарозы и скармливали пчелам с помощью встроенных в улей кормушек, обычно используемых в пчеловодстве. (B) Экстракты Fomes и Ganoderma значительно снижали уровни DWV и LSV в полевых испытаниях с использованием 5-рамочных колоний с пчелами, выделенными из общей популяции. У пчел отбирали пробы на уровень вирусов в начале лечения и через 12 дней. В колониях, получавших экстракты G. resinaceum, наблюдалось в 79 раз большее снижение DWV и в 45 000 раз большее снижение LSV по сравнению с контрольной группой, получавшей сахарный сироп. Количественные значения ПЦР ΔCt нормализованы до средних начальных уровней вируса во всех группах.
Изображение в натуральную величину
В дополнение к продемонстрированной противовирусной активности экстрактов мицелия полипоровых грибов, экстракты из не инокулированного субстрата для выращивания грибов (березовая древесина) также показали некоторую активность против DWV и LSV. Несмотря на то, что на березовых опилках не было видно видимых признаков грибковой инфекции (см. Дополнительный рис. S1), многие или большинство свободно живущих лесных деревьев имеют загадочных эндофитных и сапрофитных грибковых ассоциатов32,33, и многие из этих симбиотических эндофитов обеспечивают преимущества пригодности для хозяина34,35. Чтобы оценить эту возможность, образцы березовых опилок из этого исследования были проанализированы с использованием секвенирования следующего поколения, и было обнаружено присутствие нескольких видов грибов. На три распространенных гриба, ассоциированных с березой, приходилось 99,5% всех выявленных случаев: Graphostroma platystoma, Chondrostereum purpureum и Trametes versicolor. Это повышает вероятность того, что сапрофитные и эндофитные грибы, совместно экстрагированные с березовой древесиной, могли способствовать активности, обнаруженной в экстрактах, в том числе в необработанной березовой древесине. Необходимы дальнейшие исследования, чтобы оценить роль этих грибов в отношении любой активности по отношению к вирусам, вызываемой внутренними фитохимическими веществами березы, такими как бетулиновая кислота36,37.
Это исследование демонстрирует, что экстракты нескольких полипоровых грибов снижают титры РНК-вируса у медоносных пчел in vivo. Сообщалось, что вирусы, включая группы DWV и LSV, играют значительную роль в глобальной модели ухудшения здоровья медоносных пчел7,9,10,11,12,13, но в настоящее время для пчеловодов не доступны одобренные противовирусные материалы. Вирусы, обычно ассоциируемые с медоносными пчелами, широко распространены среди диких опылителей, не являющихся Apis, 38, что подчеркивает важность разработки средств борьбы с вирусными инфекциями в управляемых популяциях. Протестированные здесь экстракты мицелия активны при приеме внутрь и легко потребляются пчелами, что позволяет предположить потенциальное применение для пчеловодов, оказывающих критически важно. В дополнение к потенциальному прямому воздействию на здоровье медоносных пчел, противовирусная активность экстрактов грибов может стать исследовательским инструментом для дальнейшего изучения сложных взаимодействий между клещами, вирусами и здоровьем медоносных пчел.
Источник https://www.nature.com/articles/s41598-018-32194-8
|
| |
| |
|
